
主备人:张宁梅 通讯稿撰写:朱旭文
2017年9月13日上午,高二化学备课组(高考)的老师们在高二化学办公室开展了本学期第3次集体备课活动。
本次备课是由张宁梅老师主备“研究有机物的一般步骤和方法”、“脂肪烃”两节内容。张宁梅老师提前做好了非常充分的准备工作,就教材、学情进行了分析,并且提出了自己的备课建议和思路。其中建议增加的内容有:1、补充二烯烃的D-A反应;2、补充烯烃的臭氧氧化的相关内容。根据江苏高考的特点和要求,建议简略处理的内容有:1、红外光谱相关内容;2、命名中较难较烦的内容。
戴建良老师和张宁梅老师还提前预览了配套练习,将练习中一些不合适的内容进行了删减处理。
经过讨论,大家对下一部分教学内容的深度和广度有了更好的把握。
附1:主要内容:
第一章 认识有机化合物
第四节 研究有机化合物的一般步骤和方法
第二章 烃和卤代烃
第一节 脂肪烃——烷烃、烯烃和二烯烃
一、教学目标
主题1 有机化合物的组成与结构与性质
| 内容标准 | 学习要求 | 教学建议 |
| 1.了解研究有机化合物的一般步骤和方法。 | 1.复习研究有机化合物的分离提纯手段如蒸馏、萃取和分液。通过实验介绍了解重结晶、色谱法是实验室、工业中分离提纯有机物的基本方法, | 通过实际实验、实验数据、谱图的展示等给出例子的形式帮助学生理解掌握。 |
| 2.了解元素定性、定量分析确定实验式的方法,掌握通过实验数据确定实验式的方法。 | ||
| 3.了解质谱图的简单原理,掌握通过质谱图确定有机物分子式的方法。 | ||
| 4.了解通过化学方法或者红外光谱、核磁共振氢谱测定有机化合物结构的一般原理,掌握由有机物分子式通过化学方法或谱图确定有机分子结构的方法。 | ||
| 2.掌握烷烃、烯烃和二烯烃的物理、化学性质, | 5.通过对典型一系列烷烃、烯烃熔沸点、密度数据的分析,总结归纳有机化合物物理性质的变化规律,了解同分异构体物理性质变化的一般规律。 | 数据分析归纳烷烃物理性质的递变规律。 通过实验录像和演示实验让学生体验烷烃取代反应和烯烃加成反应的差别,通过反应过程的分析帮助学生加深对这两类反应本质的理解。 |
| 6.通过对烷烃、烯烃典型化合物化学性质的学习,归纳总结烷烃、烯烃化学性质的一般规律,掌握根据分子内烷、烯结构片段的识别推测其所具有的一般化学性质,进一步强化同系物通式、物理性质的递变规律和化学性质的相似性。引入烯烃的顺反异构。 | ||
| 8.理解氧化、取代、加成、加聚等有机反应类型,并能够区分它们相互的差别。引入加成反应的马氏规则和二烯烃的1,2-加成、1,4-加成。 |
二、内容分析
1、地位与功能
这两节内容是选修5第1章最后一节和第2章第一节的内容。是在学生已具备了有机物结构和命名初步知识的基础上,进一步深入学习分离提纯有机物并对其组成和结构加以分析,从而达到让学生掌握根据实验数据及谱图分析研究有机化合物组成和结构的方法。是在学生已具备烷烃和乙烯性质的基础上,进一步学习烷烃和烯烃物理性质的递变规律和化学性质的相似性,从而让学生掌握根据有机物的结构特点归纳推演性质的方法。
2、内容的选择与呈现
在学习了有机物官能团的结构和名称以及有机物结构特点及同分异构现象的基础上,本章最后一小节引入了有机物分离提纯的实验方法,介绍高一已经学习的蒸馏和萃取在有机物分离提纯中的应用,并新引入重结晶和色谱法分离提纯有机物。在高一已经了解了燃烧法测定有机物组成的基础上,大致介绍了质谱、红外光谱和核磁共振氢谱的原理,重点介绍了这三种方法在确定有机物结构中的应用。
在高一学生已经了解了甲烷、乙烯等典型有机化合物代表物的结构与性质的基础上,第二章一开始便引出同系物的概念,介绍同系物物理性质的递变规律。并通过回顾乙烷和乙烯化学性质,在已有知识的基础上归纳总结烷烃和烯烃这两类同系物的化学性质,并通过实验和反应过程的介绍,对比取代和加成反应的差别,加深学生对有机反应类型的理解,新引入了烯烃加成反应的马氏规则和二烯烃化学性质的学习,既让学生体会到和烯烃拥有相同官能团的二烯烃化学性质之间的相似性,又让学生体会到共轭二烯烃特殊的化学性质,让学生初步体会1,2-加成与1,4-加成的差别,为后续深化加聚反应的学习奠定基础。并在学生已有有机化合物分子结构特点和同分异构书写初步知识的基础上介绍烯烃的顺反异构。
三、教学建议
1、研究有机化合物的一般步骤和方法
学生已了解了结晶、蒸馏与萃取分液的实验操作。在此基础上介绍如何分离提纯有机物,可以从学生熟悉的蒸馏、萃取入手介绍这两种操作在有机化合物分离提纯中的应用,再通过分离提纯粗苯甲酸样品的实验,在学生已学过的结晶方法的基础上介绍重结晶在分离提纯有机物中的应用。
学生已经了解了有机化合物官能团的结构与名称,对甲烷、乙烯、苯、乙醇、乙酸等典型有机物的结构特点也有所认识,知道了有机物分子中呈四价的碳原子的成键特点,在此基础上介绍如何通过实验测定有机物的组成与结构,可先介绍燃烧法测定有机物的实验式帮助学生回忆,再结合高一知识介绍相对密度确定有机物的分子式。对于质谱、红外光谱和核磁共振氢谱的原理可以进行最简化的介绍,重点落在如何通过读谱确定有机物的分子式及结构,此处需要用到官能团的结构特点、碳原子的成键方式、同分异构现象、分子对称性的分析等前面所学知识,综合度较高,为本节的重难点。
教学设计案例:
第1课时:有机物的分离提纯手段
先让学生回顾:
必修1第1章我们学习了分离提纯物质的手段?请举例说明,并说出这些实验的主要使用仪器和操作注意事项。
然后介绍:
1、大家能回忆一下葡萄酒中的乙醇应该用哪种分离手段加以分离呢?这一实验方法又有哪些需要注意的地方?
流程: 蒸馏 加CaO吸水
![]()
![]() 含杂工业乙醇 95%工业乙醇 蒸馏 99.5%以上无水乙醇
含杂工业乙醇 95%工业乙醇 蒸馏 99.5%以上无水乙醇
2、大家能回忆一下西红柿中的茄红素应该用哪种分离手段加以分离呢?这一实验方法有哪些需要注意的地方?
3、含泥沙和苯甲酸钠的粗苯甲酸可以通过怎样的实验操作加以分离?
晶体
![]()
![]() (产品)
(产品)
![]()
![]()
![]() 滤液冷却,结晶,
滤液冷却,结晶,
过滤,洗涤
加热溶解 趁热过滤
![]()
![]()
![]() 固体混合物 饱和溶液溶剂稍过量防止损失 母液
固体混合物 饱和溶液溶剂稍过量防止损失 母液
(可溶性杂质
和部分被提纯物)
![]() 残渣(不溶性杂质)
残渣(不溶性杂质)
4、彼此互溶、熔沸点和溶解性相近的叶绿素、叶黄素又该如何分离呢?
例:某工厂废液经测定得知主要含有乙醇,其中还溶有丙酮、乙酸和乙酸乙酯。根据各物质的性质(如下表),确定通过下列步骤回收乙醇和乙酸。
物质丙酮、乙酸乙酯、乙醇、乙酸的沸点(℃)分别是:
56.2 ℃、77.06 ℃ 、78 ℃ 、117.9 ℃
①向废液中加入烧碱溶液,调整溶液的pH=10
②将混和液放入蒸馏器中缓缓加热
③收集温度在70~85℃时的馏出物
④排出蒸馏器中的残液。冷却后向其中加浓硫酸(过量),然后再放入耐酸蒸馏器进行蒸馏,回收馏出物
请回答下列问题:
(1)加入烧碱使溶液的pH=10的目的是 ;
(2)在70~85℃时的馏出物的主要成分是 ;
(3)在步骤④中,加入过量浓硫酸的目的是(用化学方程式表示)________________________
(4)当最后蒸馏的温度控制在85~125℃一段时间后,残留液中溶质的主要成分是 。
第2课时:有机物结构的确定
![]() 有机物粗产品 纯净有机物(纯度测定) 实验式(最简式)
有机物粗产品 纯净有机物(纯度测定) 实验式(最简式)
![]()

![]() 二、分子式的确定
二、分子式的确定
1、元素分析→确定实验室
有机物元素定量分析——“李比希元素分析法”的原理:
![]()
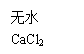
![]()
![]()

![]()

![]()
![]()
![]()
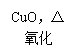
![]() 取定量含
取定量含
![]()
![]()
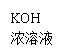 C、H(O)
C、H(O)
![]()
![]() 的有机物
的有机物
![]() 2、有机物分子式的确定方法:
2、有机物分子式的确定方法:
① 最简式法:![]() T有机物化学式(分子式):(CxHyOz)n
T有机物化学式(分子式):(CxHyOz)n
② 直接法
密度(或相对密度)→摩尔质量→1mol气体中元素原子各为多少摩尔→分子式
M = 22.4L/mol ▪ρg/L=22.4ρ g/mol
M1 =DM2(D:相对密度)
③ 余数法:
④ 质谱法
分子式→计算缺氢指数→推测可能的官能团→推测分子结构
![]()
![]() 效率较低 效率高、准确度高
效率较低 效率高、准确度高
化学实验验证官能团的化学性质 红外光谱或核磁共振氢谱测定结构
三、分子结构的鉴定
1、分子结构的鉴定的常用方法
(1)化学方法:利用特征反应鉴定出特征原子团(官能团),再制备它的衍生物进一步确定(对量有限制)
(2)物理方法:红外光谱、紫外光谱、核磁共振氢谱、X射线晶体衍射法……
2、红外吸收光谱的原理:确定有机化合物中的官能团
3、核磁共振氢谱的原理:处在不同化学环境中的氢原子因产生共振时吸收电磁波的频率不同,在谱图上出现的位置也不同,这种差异叫化学位移δ。
例题:1、同温同压下,某气体对氢气的相对密度为22。
⑴若该气体为烃,它的分子式为_____。
 ⑵若该气体为碳氧化合物,它的分子式为_____。
⑵若该气体为碳氧化合物,它的分子式为_____。
⑶该气体的分子式还可能为_______。
2、确定烃的分子式,如相对质量为58烃的分子式
3、(1)某含C、H、O三种元素的未知物A,经燃烧分析实验测定A中碳的质量分数为54.53%,氢的质量分数为9.15%,求A的实验式。
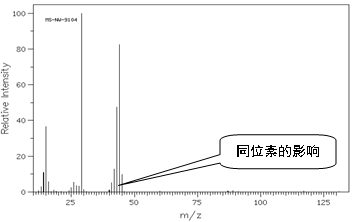
(2)已求出A的实验式是C2H4O,又知其质谱图如下,求A的分子式、可能的结构式:
A的分子式:C2H4O
A的缺氢指数(Ω)=1
A可能的结构:
(3)分子A(C2H4O)的结构是: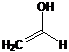 ,则核磁共振氢谱如图将有几条谱线?
,则核磁共振氢谱如图将有几条谱线?
2、第二节 脂肪烃
学生已经学习了甲烷、乙烯等典型的有机化合物,了解了它们的主要性质以及在人们生活、化工生产中的作用;重点学习了取代反应、加成反应的反应特点;初步了解了有机化合物分子结构对其性质的影响,认识了一些有机物对于人类日常生活、身体健康的重要性,初步形成了对有机化学的学习兴趣。
在此基础上,本节教学设计主要是从学生已有的知识水平出发,学习烷烃、烯烃物理性质的递变规律以及烷烃、烯烃和二烯烃的化学性质。在前面所学同分异构及有机分子结构特点的基础上介绍烯烃的顺反异构。可以通过归纳总结帮助学生深入了解烷烃的取代反应和烯烃的加成反应的区别,并进一步介绍烯烃的马氏规则,通过相似和对比帮助学生理解和二烯烃的1,2-加成和1,4-加成,并复习加深学生对于烯烃加聚反应的理解与应用。
教学设计案例:
第1课时:烷烃与烯烃的性质
介绍烷烃和烯烃的物理性质,数据分析归纳总结烃的物理性质变化规律。复习乙烷、乙烯的结构和化学性质,对比乙烷和氯气的取代反应和乙烯和溴水的加成反应,推演出烯烃的化学性质,通过丙烯和氯化氢的反应介绍马氏规则,可习题中补充高锰酸钾和臭氧对烯烃的氧化反应。
对取代反应和加成反应的认识:
1、取代反应:
可逆反应、链式反应,卤化氢的产生,多种有机物产物的产生都是学生忽略的问题:
例1:1mol烃与2molHCl发生加成反应完全,加成反应的产物能与4molCl2发生取代反应,求该烃的分子式
2、加成反应:
马氏规则的本质是需要学生关注烯烃分子的结构和加成后的同分异构现象。
例2:通常,烷烃可以由相应的烯烃经催化加氢得到。但是,有一种烷烃A,分子式C9H20,它却不能由任何C9H18的烯烃催化加氢得到。而另有A的三个同分异构体B1、B2、B3,却分别可由而且只能由1种自己相应的烯烃催化加氢得到。A、B1、B2、B3的结构简式如下(请填空):
第2课时:烯烃的顺反异构和二烯烃的性质
要求学生掌握具有顺反异构体的烯烃的结构特点、二烯烃两种加成方式以及以此为基础引申的两种加聚方式。
改课时可在苯环结构的基础上简单介绍一下双键的共轭现象,以此帮助学生复习苯环的结构为后续的学习打基础。是否补充D-A反应?
教学设计案例:
引课:思考C4H8有可能的异构体?
一、烯烃的顺反异构
(1)异构体的种类:结构异构体、空间异构体
(2)结构异构体:碳链异构、位置异构、官能团异构
(3)空间异构体:顺反异构、镜像异构
练习:C4H8有可能的异构体?
二、二烯烃
(1)概念:链烃分子里含有两个碳碳双键的不饱和烃叫做二烯烃。
(2)二烯烃的通式: CnH2n-2 (n≥3)
(3)分类:孤立二烯烃(性质与单烯烃类似) 累积二烯烃(不稳定) 共轭二烯烃(结构稳定、性质特殊)
(4)共轭二烯烃的结构
(5)共轭二烯烃的特殊性质
讨论:CH2=CH-CH=CH2与水以1∶1加成,所得产物有几种?
CH2=CH-CH=CH-CH=CH2与氯气 1∶1反应,有几种产物?
CH2=CH-CH=CH2相互加成,所得产物有几种?
例、工程塑料 ABS 树脂(结构简式如下),广泛用于汽车、建筑材料、电器制品,合成时用了三种单体。ABS:
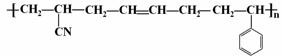
⑴这三种单体的结构简式分别是__、____、___。
⑵ABS工程树脂,这三种单体的相对分子质量由小到大的排列顺序,其符号依次表示为A、B和S按一定配比共聚而得。A、B和S三种单体中,碳氢比(C:H)值最小的单体是 。
⑶经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数), 则原料中A和B的物质的量之比是 (用a、b、c表示)。