
主备人:朱旭文 陈文婷 通讯稿撰写:陈文婷
2017年10月10日上午,高二化学备课组(小高考)的老师们聚集在汇贤楼二楼接待室,开展了本学期第6次集体备课活动。
首先朱旭文老师主讲了“铝及其化合物”复习建议,从①2017学业水平测试考试说明中有关“钠及其化合物的”的要求②教学建议③复习时的思考题这三个方面进行了阐述。建议上课时可从1、铝箔加热的现象可说明什么?2、向氯化铝溶液中逐滴加入氢氧化钠溶液,请写出依次发生反应的化学方程式。3、实验室制取氢氧化钠的方法是什么?为什么不用氢氧化钠?等情景展开复习。
接着陈文婷老师主讲了“铁及其化合物”复习建议,重点强调了关于学生计算能力的培养,这一部分内容在小高考中的计算要求很高。以2017年真题26题为例,本题中考到了极限计算、混合物计算,以及反应先后顺序的计算。
最后戴建良组长和大家讨论了期中考试的命题内容:只考已复习过的内容;命题形式:真题形式。大家一致同意。
戴建良、陈益、陈文婷、赵永承、徐守兵、王海富、朱旭文老师参加了本次备课活动。
附1:活动内容
“铝及其化合物”复习建议
朱旭文
一、2017学业水平测试考试说明中有关“钠及其化合物的”的要求
1、了解铝等金属及其重要化合物的主要用途(B)
2、了解铝等金属及其重要化合物的主要物理性质(B)
3、了解铝分别与氧气、水、酸、碱、盐等物质的反应(B)
4、了解氧化铝分别与水、酸、碱等物质的反应(B)
5、了解氢氧化铝的两性;了解氢氧化铝的受热分解(B)
二、教学建议
1.Al及其化合物间的相互转化关系图
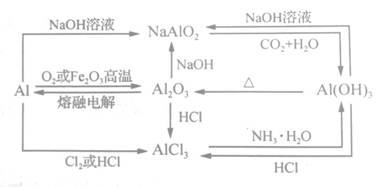
引导学生通过上述转化关系图,系统梳理铝及其重要化合物的性质。
2、教材重要实验的梳理
实验1:铝箔加热P48
实验2:铝片分别与盐酸、氢氧化钠反应 P51
实验3:氢氧化铝的制法 P58
实验4:氢氧化铝的两性P58
三、复习时的思考题
1、铝箔加热的现象可说明什么?
2、向氯化铝溶液中逐滴加入氢氧化钠溶液,请写出依次发生反应的化学方程式。
3、实验室制取氢氧化钠的方法是什么?为什么不用氢氧化钠?
|
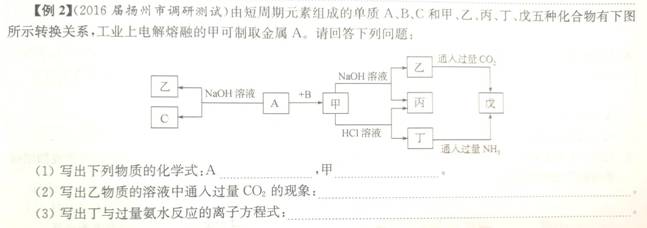
例2

“铁及其化合物”复习建议
陈文婷
一、2017学业水平测试考试说明中有关“铁及其化合物的”的要求
1、了解铁等金属及其重要化合物的主要用途(B)
2、了解铁等金属及其重要化合物的主要物理性质(B)
3、了解氧化铁等金属氧化物分别与水、酸、碱等物质的反应(B)
4、了解Fe3+的氧化性,认识Fe3+ 和Fe2+相互转化(B)
学生实验测试内容
1.探究金属铁及其化合物的性质
二、教学建议
1.Fe及其化合物间的相互转化关系图
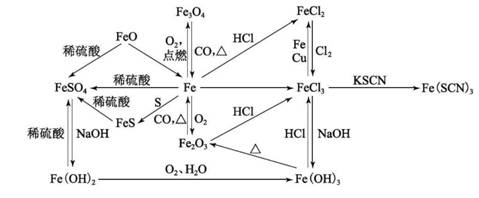 |
引导学生通过上述转化关系图,系统梳理钠及其重要化合物的性质。
2、教材重要实验的梳理
实验1:铁的燃烧 初中 实验2:钠和水的反应
实验3:铁盐、亚铁盐与碱的反应 实验4:Fe3+的检验
三、复习内容见白皮书
难点:相关计算
26.(10分)铁黑(Fe3O4)是常见的铁系颜料。一种制取铁黑的实验流程如下图所示:

制取铁黑的反应原理可表示为
Fe(OH)2 + 2Fe(OH)3 ![]() Fe(OH)2·2Fe(OH)3
Fe(OH)2·2Fe(OH)3 ![]() Fe3O4
Fe3O4
(1)加入氨水调pH至7~9时,发生反应的离子方程式为 。
(2)为了保证铁黑样品的质量,“合成”中需要控制的因素有 (填三个)。
(3)铁黑产品中Fe3O4的含量是判断产品等级的依据之一。某铁黑样品中混有的杂质为FeO、Fe2O3中的一种。根据国标方法,进行的测定实验如下:
步骤1:称取1.908g样品置于锥形瓶中,加入足量盐酸,加热使之完全溶解。
步骤2:向锥形瓶中先加入足量的SnCl2溶液,将Fe2+全部转化为Fe2+,除去过量的Sn2+,再加入一定量的硫酸和磷酸,并滴加指示剂。
步骤3:再向锥形瓶中滴加0.08200mol·L—1K2Cr2O7溶液,发生反应:
Cr2O72—+ 6Fe2+ + 14H+ =2Cr3+ + 6Fe3+ + 7H2O
恰好完全反应时,共消耗50.00mLK2Cr2O7溶液。
请计算样品中Fe3O4的质量分数(写出计算过程)。
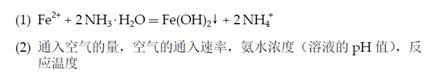 答案:
答案:
 |
(3)